Vědci objevili skrytý molekulární spínač, který řídí chuť, metabolismus i funkci střev
 Foto: Ilustrační_ kalhh/Pixabay
Foto: Ilustrační_ kalhh/PixabayPřipravit, vypnout, nenajíždět na lednici! Představte si, že máte v těle spínač, kterým můžete ovládat své chutě. Nebylo by to báječné?
Vědci z Northwesternské univerzity totiž objevili skrytý „řídicí spínač“, který se nachází uvnitř proteinu. Jeho skrytá funkce je velmi přínosná. Pomáhá totiž tělu vnímat chuť, kontroluje hladinu cukru v krvi a dokonce chrání střeva. Dokáže zapnout, vypnout, nebo dokonce přebít klíčový protein přímo v buňkách.
Tento přepínač se nachází uvnitř proteinu TRPM5. Může fungovat stejně jako akcelerátor, ale také jako brzda. Důležitá je závislost na molekule, která se na něj váže.
Vědci dosud předpokládali, že TRPM5 se může aktivovat pouze tehdy, když se uvnitř buněk zvýší hladina vápníku. Nová studie však odhaluje, že malé molekuly můžou protein přímo ovládat! A vápník k tomu vůbec není potřeba.
Vědci identifikovali dvě molekuly. Jednu, kteráTRPM5 aktivuje a druhou, která se váže na přesně stejné místo, ale zároveň ji vypíná, což odhaluje systém dvojího použití.
Protože TRPM5 hraje klíčovou roli v biologických procesech, které propojují chuť, metabolismus a zdraví střev, otevírá tak nové možnosti terapeutického vývoje. Mezi potenciální aplikace patří zvýšení uvolňování inzulínu pro zlepšení kontroly glukózy u diabetu, modulace vnímání chuti pro omezení chuti na jídlo a regulace imunitní signalizace střeva pro snížení zánětu.
„TRPM5 se podílí na metabolických poruchách, včetně diabetu 2. typu a obezity. Pokud vědci dokážou identifikovat léky, které tento kanál aktivují, mohli by podpořit produkci inzulínu k léčbě onemocnění, které mají problémy s tvorbou inzulínu.
Nyní, když vědci znají celkovou architekturu TRPM5 a vědí, jak jej aktivovat a inhibovat, poskytují tím základ pro budoucí vývoj léků.
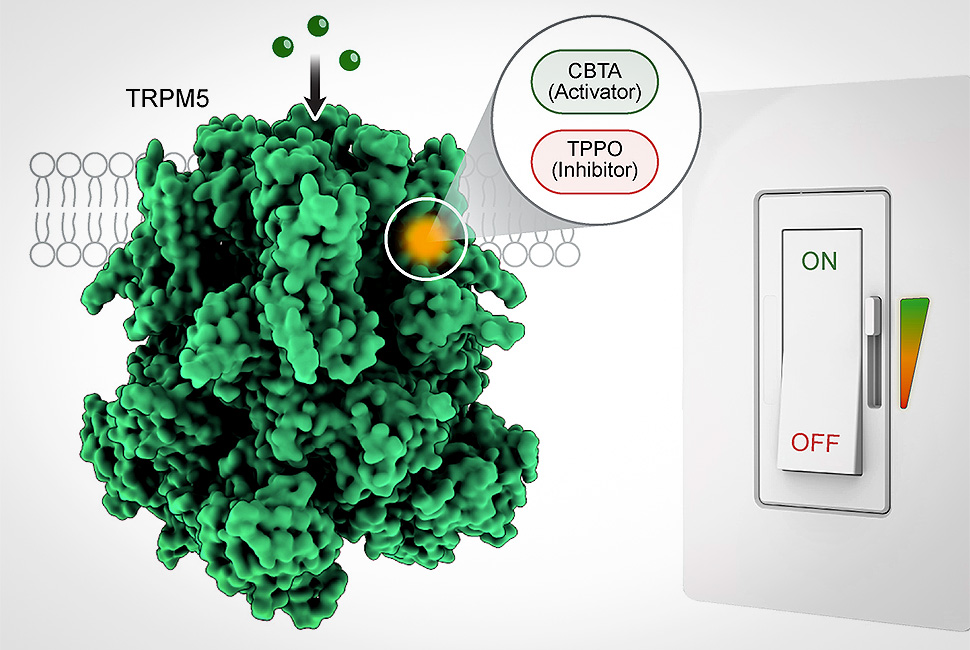 Foto: Juan Du/Wei Lu/Northwesternská univerzita_tiskový zdroj
Foto: Juan Du/Wei Lu/Northwesternská univerzita_tiskový zdrojTRPM5 působí jako zesilovač signálu a nachází se uvnitř mnoha typů buněk. Když je otevřený, umožňuje průtok sodíkových iontů, což pomáhá buňkám vysílat elektrické signály, které řídí klíčové biologické procesy. Na jazyku pomáhá detekovat sladké, hořké a umami chutě. Ve slinivce břišní podporuje uvolňování inzulínu po jídle. A ve střevě pomáhá vnímat živiny a regulovat imunitní obranu.
Tým také zjistil, že když molekula aktivuje TRPM5, stává se extra citlivou na vápník a reaguje na drobné změny, které by ji normálně neovlivnily. To ukazuje, že kapsa protein nejen řídí, ale může ho i velmi rychle nabít.
Zdroje: https://www.nature.com/articles/s41589-025-02097-7; studii vedl Wei Lü ze společnosti Northwestern spolu s Juanem Duem, https://news.northwestern.edu/stories/2026/01/hidden-molecular-switch-controls-taste-metabolism-and-gut-function?fj=1


 Foto: David_SMC/Pixabay
Foto: David_SMC/Pixabay Foto: Jesse Lai, Ichida Lab/AAAS/CC BY-SA
Foto: Jesse Lai, Ichida Lab/AAAS/CC BY-SA Foto: S laskavým poděkováním Joshimu Berlindovi/CC BY-SA
Foto: S laskavým poděkováním Joshimu Berlindovi/CC BY-SA
 Foto: tabitha turner/unsplash
Foto: tabitha turner/unsplash

 Foto: julientromeur/Pixabay
Foto: julientromeur/Pixabay Foto: Iveta Mauci/Obrázek vytvořený pomocí AI
Foto: Iveta Mauci/Obrázek vytvořený pomocí AI Foto:
Foto: 

 Foto: PublicDomainPictures/Pixabay
Foto: PublicDomainPictures/Pixabay Foto: Joshua J. Cotten/Pixabay
Foto: Joshua J. Cotten/Pixabay Foto: SALK INSTITUTE
Foto: SALK INSTITUTE